10/5 Kémia 1. epocha (4-5. óra - Oldatok, oldhatóság)
Tovább>>
4. óra
Oldatok (Tk.: 74-87.o.)
FELADAT:
1. Töltsd ki a táblázat hiányzó adatait!
Az oldatok összetett anyagok, keverékek, amelyek oldószerből és oldott anyagból állnak.
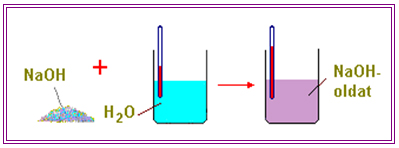
| Oldat neve | Oldószer | Oldott anyag |
| NaOH-oldat | ||
| Sóoldat | ||
| víz | citromlé | |
| kakaópor | ||
| Porleves | ||
| jód | ||
| Kávé | ||
| . |
2. Tömegszázalék - töltsd ki a táblázat hiányzó adatait!
Az oldatok összetételét többféleképpen fejezhetjük ki. Az egyik lehetőség a tömegszázalék (jele: m/m%). A tömegszázalék megmutatja, hogy 100 g oldatban hány gramm oldott anyag van!
|
Oldat tömege |
Oldott anyag tömege |
Oldószer tömege |
Tömegszázalék |
|
100 g |
|
|
10 m/m% |
|
200 g |
|
|
10 m/m% |
|
300 g |
60 g |
|
|
|
400 g |
|
300 g |
|
|
|
40 g |
160 g |
|
|
|
20 g |
|
50 m/m% |
|
|
|
360 g |
10 m/m% |
3. Hány tömegszázalékos az az oldat, amelynek
A) 300 g-ja 60 g oldott anyagot tartalmaz?
B) 400 g-ja 20 g oldott anyagot tartalmaz?
4.Hány gramm oldott anyagot tartalmaz
A) 250 g 20 m/m%-os oldat?
B) 900 g 25 m/m%-os oldat?
5. Hány gramm oldószer van
A) 300 g 15 m/m%-os oldatban?
B) 500 g 20 m/m%-os oldatban?
6.Hogyan készítenél
A) 600 g 15 m/m%-os cukoroldatot?
B) 300 g 30 m/m%-os sóoldatot?
7. Hány gramm 5 m/m%-os sóoldat készíthető
A) 120 g sóból?
B) 78 g sóból?
PLUSZfeladat:
KÖVETELMÉNY:
Az oldat összetevőinek ismerete.
Egyszerű tömegszázalékos feladatok.
Fogalmak: oldat, oldószer, oldott anyag, telítetlen oldat, telített oldat, túltelített oldat.
INTERAKTÍV:
Oldatok>>
5. óra
Oldhatóság
FELADAT:
1. Az oldódás sebessége (oldódási sebesség) számos módon gyorsítható. Emlékezz vissza, hogyan tudod elősegíteni, hogy a teában gyorsabban oldódjon fel a cukor?
2. Húzd alá, mely tevékenységekkel lehet gyorsítani az oldódás sebességét?
A) Növeljük az oldószer hőmérsékletét*
B) Aprítjuk az oldandó anyagot
C) Napfényre tesszük az oldatot
D) Kevergetjük az oldatot
E) Műanyagpohárban végezzük az oldást
3. Egészítsd ki a mondatot!
Az oldódás sebessége a hőmérséklet emelésével általában.............
4. feladat
100 g víz 20 Celsius fokon 36 g konyhasót képes feloldani. Mit jelent ez?
A) Mekkora lehet a 20 Celsius-fokos víz maximális tömegszázaléka? (Ügyelj, hogy a 100 g nem az oldatra, hanem a víz mennyiségére utalt!)
B) Mi történik, ha 100 g vízben 20 Celsius-fokon több, mint 36 g konyhasót oldunk?
C) Mit jelentenek az alábbi fogalmak: telített oldat, telítetlen oldat, túl telített oldat?
D) Mi történik, ha a 20 Celsius-fokon telített konyhasóoldatot 5 Celsius-fokosra hűtjük?
5. Töltsd ki a táblázat hiányzó adatait! A vizsgált oldat 25 Celsius-fokon maximálisan 30 m/m%-os lehet.
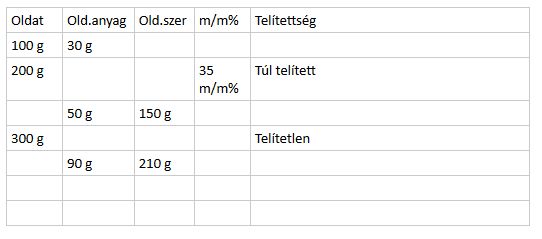 6. Hasonlítsd össze, az alábbi oldatpárokat! Jelöld melyik a töményebb (T), melyik a hígabb (H)
6. Hasonlítsd össze, az alábbi oldatpárokat! Jelöld melyik a töményebb (T), melyik a hígabb (H)
A) 100 g 10 m/m%-os sóoldat - 200 g, 25 g cukrot tartalmazó cukoroldat
B) 200 g 30 g oldott anyagot tartalmazó oldat – 200 g 180 g oldószert tartalmazó oldat
C) 200 g vízből és 20 g cukorból álló cukoroldat – 150 g 12 m/m%-os sóoldat
7. Hogyan nevezzük az alábbi változásokat?
A) 200 g 15 m/m%-os oldathoz hozzáadunk 40 g vizet.
B) 180 g 12 m/m%-os oldatból elpárologtatunk 18 g vizet.
*8.Olvasd le a grafikonról, hogy mekkora a konyhasó oldhatósága (x g só / 100 g víz) 20oC-on és 80 oC-on!
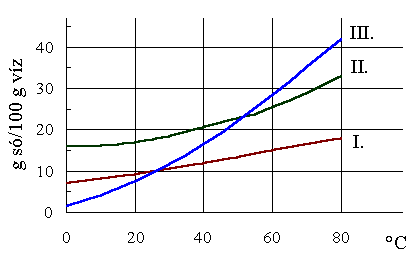
*9. Hány tömegszázalékos a telített sóoldat 20 illetve 80 oC-on? tömeg% = (oldott anyag tömege/oldat tömege) x 100
*10. Figyeld meg az egyes anyagok oldódását különböző hőmérsékleteken! Mit veszel észre?
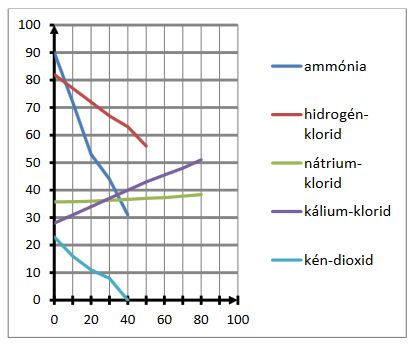
A gázok a hőmérséklet emelésével ................................................................... oldódnak.
A szilárd anyagok általában a hőmérséklet emelésével ................................ oldódnak.
A konyhasó oldódása a hőmérséklet emelésével ...........................................................
PLUSZfeladat:
Oldd meg a *8, *9, *10 feladatokat!
KÍSÉRLETEK
I. Sóoldat készítése
Szükséges eszközök, anyagok: 50 ml-es főzőpohár, üvegbot, mérőhenger, konyhasó, tálca, óraüveg
20 ml vízben oldjatok fel 1 g konyhasót! Az elkészült oldatot takarjátok le (óraüveg), a következő órán szükségetek lesz rá!
II. Túl telített oldat készítése
Szükséges eszközök, anyagok: 250 ml-es főzőpohár, üvegbot, mérőhenger, vasháromláb, azbesztháló, réz-szulfát, tálca, hurkapálca, cérna
!Figyelem! A réz-szulfát maróanyag, viselj védőszemüveget!
100 ml vizet kezdjetek el óvatosan melegíteni! Fokozatosan, kevergetés mellett oldjatok fel benne 50 g réz-szulfátot. Ha befejeztétek lógassatok az oldatba cérnát, amelyet a hurkapálcika segítségével rögzítetek a főzőpohár tetején. Tegyétek olyan helyre, ahol nem piszkálja senki a következő óráig!
*III. Rögzítsétek az előző kísérleteket fényképen, filmen!
IV. Bepárlás
Szükséges eszközök: vasháromláb, Bunsen-égő, azbesztháló, 250 ml-es főzőpohár, Petri-csésze (főzőpohár méretű).
Mérjétek le a főzőpohárra helyezendő óraüveg tömegét!
Öntsetek a főzőpohárba kb. 100 ml vizet, helyezzétek rá az óraüveget. Az óraüvegbe töltsetek az I. kísérletben elkészített sóoldatból, majd kezdjétek el melegíteni a főzőpoharat. Párologtassátok el a tegnapi sóoldat egészét.
Mérjétek meg a kivált só és az óraüveg össztömegét, majd számoljátok ki a kivált só mennyiségét! Változott-e a tegnapihoz képest?
V. Kristályosítás
Nézzétek meg mi történt egy nap elteltével a II. kísérletben készített oldattal!
GYAKORLÓ FELADATOK:
I. Szint
10. Mekkora a keletkező oldat tömegszázalékos összetétele, ha
A) 300 g 17 m/m%-os sóoldahoz 120 g vizet öntünk.
B) 730 g 21 m/m%-os cukoroldathoz 70 g vizet öntünk.
C) 1,5 kg 19 m/m%-os sóoldathoz 900 g vizet öntünk.
11. Mekkora a keletkező oldat tömegszázalékos összetétele, ha
A) 760 g 15 m/m%-os cukoroldatból elpárologtatunk 80 g vizet.
B) 130 g 28 m/m%-os sóoldatból elpárologtatunk 75 g vizet.
C) 9600 g 17 m/m%-os sóoldatból elpárologtatunk 0,5 kg vizet.
II. Szint
12. Mekkora annak az oldatnak tömegszázalékos összetétele, amelyet úgy készítünk, hogy összeöntünk
A) 200 g 15 m/m%-os és 170 g 5 m/m%-os oldatot.
B) 920 g 31 m/m%-os és 170 g 15 m/m%-os oldatot.
C) 1890 g 13,5 m/m%-os és 2340 g 32,4 m/m%-os oldatot.
III. Szint
Az oldatok töménysége nemcsak tömegszázalékban adható meg. Amennyiben az oldott anyag folyadék vagy gáz gyakran alkalmazzák a térfogatszázalékot. A térfogatszázalék megadja, hogy 100 cm3 oldatban hány cm3 oldott anyag van. Mértékegysége: V/V%
Térfogat% = (oldott anyag térfogata / oldat térfogata) x 100
13. Hány térfogatszázalékos az az alkohol, amelynek
A) 200 cm3-e 20 cm3 etil-alkoholt tartalmaz.
B) 350 cm3 -e 25 cm3 etil-alkoholt tartalmaz.
C) 490 cm3-e 410 cm3 vizet tartalmaz.
14. Hány cm3 alkoholt tartalmaz 500 cm3 6 V/V%-os sör?
Fontos! Két folyadék összeöntésekor a tömegük összeadódik, a térfogatuk viszont NEM (mindig)! Ha összeöntünk 100 g vizet és 100 g alkoholt a tömegük 200 g lesz. Ha összeöntünk 100 cm3 vizet és 100 cm3 alkoholt a térfogatuk kevesebb lesz, mint 200 cm3! A folyadékok összeöntése nem egyszer kis mértékű térfogatcsökkenéssel jár.
I. szinS
15. Az oldhatósági táblázat alapján válaszolj az alábbi kérdésekre!
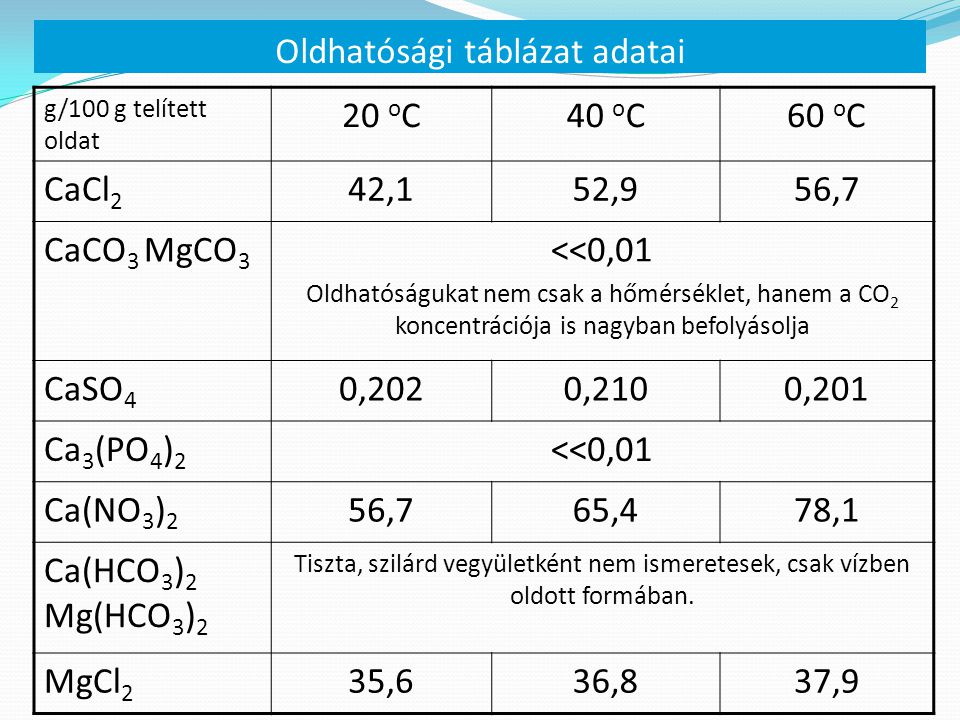
A) Hány gramm kalcium-kloridot tartalmaz 200 g, 40 C-on telített oldat?
B) Hány gramm kalcium-klorid válik ki, ha 300 g, 60 C-on telített oldatot 40 C-ra hűtünk?
C) Ábrázold a kalcium-nitrát - Ca(NO3)2 oldhatósági görbéjét a hőmérséklet függvényében!
*D) Hány gramm magnézium-kloridot kell feloldani 350 g !!!VÍZBEN!!!, 40 C-on, hogy telített oldatot kapjunk?