10/5 Kémia 1. epocha (1-3. óra - atomszerkezet, kötések, anyagi rendszerek)
Tovább
Javasolt tankönyv: Horváth Balázs, Péntek Lászlóné, Siposné Dr. Kedves Éva Dr.: Kémia 9. Általános és szervetlen kémia, Mozaik Kiadó
Értékelés:
Egyéni
Mikrodolgozat (atom- és elektronszerkezet, izotópok) 5%
Mikrodolgozat 2. (tömegszázalék) 5%
Részteszt 15%
Epochazáró 35%
Csoportos
Laboratóriumi szabályok (tűz-, munka-, balesetvédelmi) . kisfilm, plakát 5%
Kísérlet kisfilm 10%
PLUSZ feladatok 1% / feladat
1. óra
Atommodellek és az atom felépítése (Tk. 15-21.o.)
Az elektronburok szerkezete, az atomszerkezet és a periódusos rendszer (Tk. 28-35.o.)
FELADAT:
1. Írd fel az alábbi atomok elektronszerkezetét!
a) 11 Na, b) 14 Si, c) 8 O, d) 18 Ar
2. Töltsd ki a táblázat hiányzó adatait!
| Izotóp jelölése |
protonszám | elektronszám | neutronszám | tömegszám |
|
|
6 | 7 | ||
|
|
8 | 17 | ||
|
238 U |
||||
|
N |
8 | |||
|
|
6 | 12 |
3. Pótold a hiányzó szavakat!
Az atom kifelé (A).................................., mert az atommagban lévő (B)..........................száma megegyezik az elektronhéjon levő (C) ...................................számával.
Az atomok kémiai minőségét az atommagban lévő (D)....................................száma határozza meg.
A kémiai elemek (E)......................................................................épülnek fel.
A protonok és neutronok számának összege adja az atom (F)....................................................
A periódusos rendszerben az (G)........................................................megegyezik az atomjaikban lévő protonok számával.
Egy kémiai elem azonos rendszámú, de különböző tömegszámú atomjait izotópatomoknak nevezzük. Az izotópok kémiai szempontból hasonlóan viselkednek. Ez alól kivétel a hidrogénatom.
A hidrogénatomnak három izotópja van: az 1-es tömegszámú hidrogénizotóp 99,986%-ban van jelen.
Létezik még a 2-es tömegszámú deutérium, mely a nehézvíz alkotórésze.
A 3-as tömegszámú trícium is.
A klór kétféle izotópból épül fel, a szén 3-féle, a vas 4-féle, a cink 17-féle izotópot tartalmaz.
Az elektronburok (H)....................................., az elektronhéjak (I)................................................ állnak.
Azt a térrészt, ahol az elektron tartózkodási valószínűsége 90%-os, (J)............................nevezzük.
Az atom külső héját (K)...................................................................... nevezzük.
KÖVETELMÉNY:
Rendszám alapján az adott atom proton, elektron és neutron számának meghatározása.
Izotópok elemi részecskeszámának és tömegének meghatározása.
Adott atom elektronszerkezetének felírása.
Fogalmak: atom, atommag, elektronfelhő, vegyjel, elemi részecske, rendszám, tömegszám, izotóp, moláris tömeg, elektronhéj, telített elektronhéj, telítetlen elektronhéj.
PLUSZ feladat:
A Tk. 29-30. oldala segítségével áttekinthető vázlat készítése a kvantumszámokról, a Pauli-elvről és a Hund-szabályról. Ezek értelmezése és szóbeli ismertetésük.
INTERAKTÍV:
Az atom szerkezete>>
Az atom szerkezete 2.>>
Az atomok elektronszerkezete>>
2. óra
Kémiai kötések (Tk.41-51.o.).
FELADAT:
1. Készíts egy táblázatot a füzetedbe a rácstípusokról az alábbi szempontok szerint:
- szerepeljen mind a 4 rácstípus,
- jelöld milyen részecskék vannak a rácspontjaiban,
- milyen kötés alakul ki a részecskék között,
- milyen az olvadás- és forráspontja,
- oldódik-e vízben,
- vezeti-e az elektromos áramot,
- írj példát mindegyikhez!
2. Írd fel az alábbi ionok jelölését!
a) nátriumion b) kalciumion c) alumíniumion d) nitridion e) oxidion f) fluoridion
3. Írd fel az alábbi részecskék elektronszerkezetét!
a) neon b) fluoridion c) oxidion d) nátriumion e) kalciumion
4. Egészítsd ki a mondatokat!
a) Az I. főcsoport elemei leadnak egy elektront, ezáltal (A)................... pozitív töltésű ionok lesznek. Ilyen pl.: a (B).................
b) Két elektront adnak le a (C).......... főcsoport elemei, ezáltal (D) ................... pozitív töltésű ionok lesznek. Ilyen pl.: a (E).................
c) Egyszeresen negatív töltésű ionok lesznek az VII. főcsoport elemei, mert (F)................ egy elektront.
d) Kétszeresen negatív töltésű ionok lesznek a (G)................ főcsoport elemei, mert felvesznek (H)...........elektront.
KÖVETELMÉNY:
Fémes kötés kialakulásának feltételei.
Kovalens kötés kialakulása, típusai (1x, 2x,3x, poláris-apoláris).
Ionképződés, ionos kötés.
Fogalmak: fémes kötés, fémrács, atomtörzs, telítetlen elektronhéj, kovalens kötés, kötő elektronpár, szigma- és pi-kötés, polaritás, poláris és apoláris kovalens kötés, ion, anion, kation, ionkötés, ionrács.
PLUSZ feladat:
A Tk. 50-51. oldala segítségével áttekinthető vázlat készítése a kötési energia, kötéshossz, kötésszög fogalmáról. Ezek értelmezése és szóbeli ismertetésük.
INTERAKTÍV:
Alapszint:
Kötéstípusok>>
Emelt szint:
Kovalens kötés 1.>>
Kovalens kötés 2.>>
Ionkötés 1.>>
Ionkötés 2.>>
3. óra
Halmazok, anyagi rendszerek és csoportosításuk, halmazállapotok. (Tk. 38-40., 66-73)
FELADAT:
1. Készíts egy összehasonlító táblázatot a halmazállapotokról az alábbi négy, digitális oktatóanyag feldolgozásával!
És, ha ezek nem lennének elég EZ is segíthet.
2. A Tk. 66.o. segítségével tudd értelmezni az alábbi ábrákat!
Tekintsd át és értelmezd az alábbi táblázatokat!
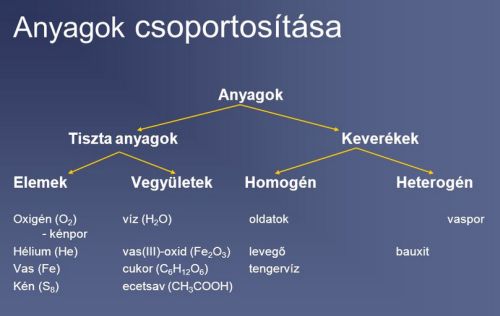
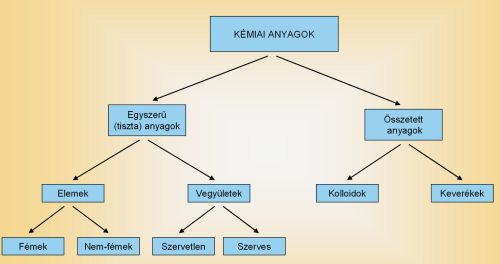
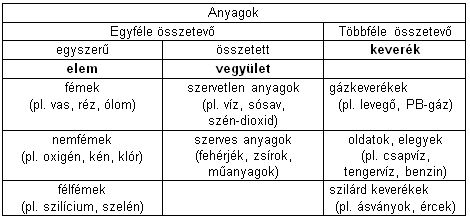
Ha ez kevés ITT van még egy.
3. Jelöld, melyek anyag ELEM, melyik VEGYÜLET, melyik KEVERÉK!
Csapvíz, vas, kén-dioxid, kőolaj, tenger víz, desztillált víz, hidrogén-klorid, oxigénmolekula, levegő, konyhasó (nátrium-klorid), magnézium, ammónia.
4. Tisztázandó az atom, elem és molekula fogalma! Mit jelent az elemmolekula és a vegyületmolekula fogalma?
5. Mit jelent az anyagmennyiség fogalma?
PLUSZfeladat:
Végezd el a 1. Halmazállapotok vizsgálata - kísérletet! A kísérletről készíts egy rövid filmfelvételt (telefonnal, hang nem kell). Magyarázd meg a tapasztaltakat!
KÖVETELMÉNY:
Fogalmak: egyszerű anyag, összetett anyag, elem, vegyület, keverék.

